Notre recherche
Au cours de la division cellulaire les chromosomes sont fidèlement dupliqués et segrégés, de telle sorte qu’un seul exemplaire de chaque chromosome soit hérité par les deux cellules filles, qui doivent porter une information génétique identique. La fidélité de la transmission des chromosomes a d’importantes implications médicales. Par exemple, un nombre aberrant de chromosomes dans les cellules germinales (ovule ou spermatozoïde) génère des embryons qui soit avortent spontanément, soit présentent des pathologies graves comme le syndrome de Down (trisomie 21). Par ailleurs, le partage inégal du génome au cours des millions de divisions cellulaires qui ont lieu dans notre corps peut aussi contribuer au développement de tumeurs.
Notre laboratoire étudie les mécanismes de surveillance de l’integrité du génome fonctionnant pendant la mitose, en utilisant la levure Saccharomyces cerevisiae comme organisme modèle.
En particulier, nous nous concentrons sur deux aspects de la mitose qui sont indispensables pour éviter l’aneuploïdie :
- Comment la fidélité de la séparation des chromosomes est supervisée par le « spindle assembly checkpoint » (SAC), qui surveille l’attachement correct des chromosomes au fuseau mitotique,
- Comment la sortie de la mitose et la cytocinèse sont régulées afin de préserver la stabilité du génome.
Principaux projets de recherche de notre groupe
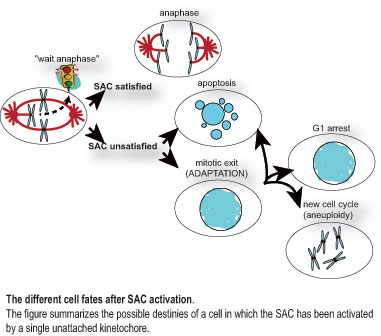
* Mécanismes renforçant l’activité du « spindle assembly checkpoint »
Le SAC empêche l’entrée en anaphase en cas d’erreur pendant le processus de bi-orientation des chromosomes sur le fuseau mitotique. En retardant la séparation des chromatides soeurs et la sortie de la mitose, le SAC fournit le temps nécessaire pour établir les connexions appropriées entre kinétochores et microtubules, assurant ainsi une partition chromosomique égale. Une fois que tous les chromosomes sont correctement bi-orientés, le SAC est satisfait et l’anaphase a lieu.
Malgré son importance, l’arrêt du cycle cellulaire induit par le SAC est une condition transitoire et, après une exposition prolongée aux poisons qui dépolymérisent les microtubules ou en présence de perturbations dans les interactions entre kinétochores et microtubules, les cellules échappent à l’arrêt du cycle cellulaire et s’adaptent. L’adaptation est considérée comme une cause majeure de la résistance des cellules tumorales aux chimiothérapies à base de composés qui interfèrent avec la fonction des microtubules (ex : paclitaxel ; vinca-alkaloids). En dépit de cela, les facteurs influençant le taux d’adaptation sont largement inconnus. Nous essayons d’identifier les gènes de levure impliqués dans l’adaptation au SAC par des cribles génétiques. En outre, nous essayons d’identifier des allèles dominants de gènes du SAC qui retardent l’extinction ou l’adaptation au SAC.
* Contrôle de la sortie de la mitose et de la cytokinèse par le « spindle position checkpoint »
Le positionnement précis du fuseau mitotique est critique pour la transmission correcte des chromosomes, en particulier dans les cellules qui se divisent de façon asymétrique. Par exemple, perturber le positionnement du fuseau dans les cellules souches conduit au développement du cancer. Chez la levure de boulangerie, qui se divise aussi asymétriquement, une position incorrecte du fuseau retarde la sortie de mitose et la cytokinèse jusqu’à ce que le fuseau soit aligné le long de l’axe mère-bourgeon. La cible de ce mécanisme est une petite GTPase appelée Tem1 qui est nécessaire à la sortie de la mitose et à la cytokinèse par l’activation d’une cascade de transduction du signal appelée « mitotic exit network » (MEN). La signalisation du MEN a lieu aux pôles du fuseau, où son orientation est surveillée par rapport aux signaux corticaux. Nous étudions les détails de la régulation de Tem1, pour ce qui concerne son activité GTPase et sa modulation par la GTPase-activating protein (GAP) a deux composants Bub2/Bfa1 dans les situations où le fuseau est mal positionné.
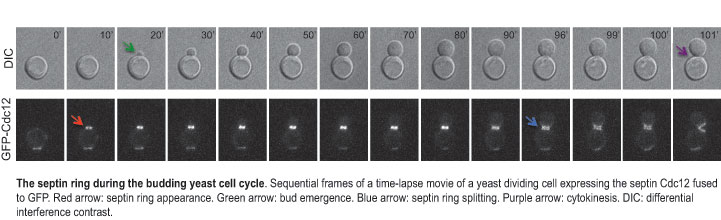
* Régulation de la dynamique des septines pendant la cytokinèse
Un faisceau croissant de preuves indique que des cellules polyploïdes sont génétiquement instables et subissent plus souvent que les cellules normales une ségrégation incorrecte des chromosomes et l’aneuploïdie, ce qui favorise le développement des cancers. Un mécanisme commun de la formation des cellules polyploïdes sont les défauts de cytokinèse. Chez les champignons et les cellules animales, la cytokinèse exige des protéines du cytosquelette appelées septines et un anneau contractile d’actomyosine. Nous avons impliqué deux ubiquitine-ligases redondantes, que nous avons appelées Dma1 et Dma2, dans le contrôle de la cytokinèse et la dynamique des septines. Grâce à des approches génétiques, nous avons identifié des cibles potentielles de Dma1 et Dma2 et sommes en train de caractériser leur rôle précis dans la dynamique des septines, ainsi que leur possible régulation par ubiquitination.
En savoir plus
Financements
FRM (Simonetta Piatti)
ANR SEPTORG (Simonetta Piatti)
Publications
2024
- Septin Organization and Dynamics for Budding Yeast Cytokinesis. Varela Salgado M, Piatti S. J Fungi (Basel). 2024 Sep 9;10(9):642. Pubmed
- Phosphorylation of the F-BAR protein Hof1 drives septin ring splitting in budding yeast. Salgado MV, Adriaans IE, Touati SA, Ibanes S, Lai-Kee-Him J, Ancelin A, Cipelletti L, Picas L and Piatti S.. Nat Commun 15, 3383 Open Access
2022
- The Syp1/FCHo2 protein induces septin filament bundling through its intrinsically disordered domain. Ibanes S, El-Alaoui F, Lai-Kee-Him J, Cazevieille C, Hoh F, Lyonnais S, Bron P, Cipelletti L, Picas L, Piatti S. Cell Rep. 41(10):111765. Pubmed
2021
- Downregulation of the Tem1 GTPase by Amn1 after cytokinesis involves both nuclear import and SCF-mediated degradation. Devault A, Piatti S. J Cell Sci. jcs.258972 Pubmed
2020
- Silencing the spindle assembly checkpoint: Let’s play Polo! Benzi G, Piatti S. J Cell Biol. 219(12):e202010053 Pubmed
- Killing two birds with one stone: how budding yeast Mps1 controls chromosome segregation and spindle assembly checkpoint through phosphorylation of a single kinetochore protein. Giorgia Benzi, Simonetta Piatti. Curr Genet. 66(6):1037-1044 Pubmed
- Cytokinesis: An Anillin-RhoGEF Module Sets the Stage for Septin Double Ring Assembly. Piatti S. Curr Biol. 30(8):R347-R349 Pubmed
- A common molecular mechanism underlies the role of Mps1 in chromosome biorientation and the spindle assembly checkpoint. Benzi G, Camasses A, Atsunori Y, Katou Y, Shirahige K, Piatti S. EMBO Rep. e50257. Pubmed
- The Phosphatase PP1 Promotes Mitotic Slippage through Mad3 Dephosphorylation. Ruggiero A, Katou Y, Shirahige K, Séveno M, Piatti S. Curr Biol. 30(2):335-343.e5. Pubmed
2019
- Septin clearance from the division site triggers cytokinesis in budding yeast. Tamborrini D, Piatti S. Microb Cell. 6(6):295-298. Pubmed
2018
- Recruitment of the mitotic exit network to yeast centrosomes couples septin displacement to actomyosin constriction. Tamborrini D, Juanes MA, Ibanes S, Rancati G, Piatti S. Nat Commun. 9(1):4308. Pubmed
2017
- Asymmetric Localization of Components and Regulators of the Mitotic Exit Network at Spindle Pole Bodies. Scarfone I, Piatti S. Methods Mol Biol. 1505:183-193. Pubmed
2016
- Control of Formin Distribution and Actin Cable Assembly by the E3 Ubiquitin Ligases Dma1 and Dma2. Juanes MA, Piatti S. Genetics. 204:205-20. Pubmed
- The final cut: cell polarity meets cytokinesis at the bud neck in S. cerevisiae. Juanes MA, Piatti S. Cell Mol Life Sci. 73:3115-36. Pubmed
2015
- Asymmetry of the budding yeast Tem1 GTPase at spindle poles is required for spindle positioning but not for mitotic exit. Scarfone I, Venturetti M, Hotz M, Lengefeld J, Barral Y, Piatti S. PLoS Genet. 11:e1004938. Pubmed
- Coupling spindle position with mitotic exit in budding yeast: The multifaceted role of the small GTPase Tem1. Scarfone I, Piatti S. Small GTPases. 6:196-201. Pubmed
- Rho1- and Pkc1-dependent phosphorylation of the F-BAR protein Syp1 contributes to septin ring assembly. Merlini L, Bolognesi A, Juanes MA, Vandermoere F, Courtellemont T, Pascolutti R, Séveno M, Barral Y, Piatti S. Mol Biol Cell. 26:3245-62. Pubmed
2013
- Budding yeast greatwall and endosulfines control activity and spatial regulation of PP2A(Cdc55) for timely mitotic progression. Juanes MA, Khoueiry R, Kupka T, Castro A, Mudrak I, Ogris E, Lorca T, Piatti S. PLoS Genet. 9(7):e1003575. Pubmed
- Yeast haspin kinase regulates polarity cues necessary for mitotic spindle positioning and is required to tolerate mitotic arrest. Panigada D, Grianti P, Nespoli A, Rotondo G, Castro DG, Quadri R, Piatti S, Plevani P, Muzi-Falconi M. Dev Cell. 26(5):483-95. Pubmed
2012
- Budding yeast dma proteins control septin dynamics and the spindle position checkpoint by promoting the recruitment of the Elm1 kinase to the bud neck. Merlini L, Fraschini R, Boettcher B, Barral Y, Lucchini G, Piatti S. PLoS Genet. 8(4):e1002670. Pubmed
- Role of the Mad2 dimerization interface in the spindle assembly checkpoint independent of kinetochores. Mariani L, Chiroli E, Nezi L, Muller H, Piatti S, Musacchio A, Ciliberto A. Curr Biol. 22(20):1900-8. Pubmed
2011
- Analysis of the rpn11-m1 proteasomal mutant reveals connection between cell cycle and mitochondrial biogenesis. Esposito M, Piatti S, Hofmann L, Frontali L, Delahodde A, Rinaldi T. FEMS Yeast Res. 11(1):60-71. Pubmed
- The mother-bud neck as a signaling platform for the coordination between spindle position and cytokinesis in budding yeast. Merlini L, Piatti S. Biol Chem. 392(8-9):805-12. Pubmed
2010
- The RSC chromatin-remodeling complex influences mitotic exit and adaptation to the spindle assembly checkpoint by controlling the Cdc14 phosphatase. Rossio V, Galati E, Ferrari M, Pellicioli A, Sutani T, Shirahige K, Lucchini G, Piatti S. J Cell Biol. 191(5):981-97. Pubmed
- Adapt or die: how eukaryotic cells respond to prolonged activation of the spindle assembly checkpoint. Rossio V, Galati E, Piatti S. Biochem Soc Trans. 38(6):1645-9. Pubmed
2009
- Cdc14 inhibition by the spindle assembly checkpoint prevents unscheduled centrosome separation in budding yeast. Chiroli E, Rancati G, Catusi I, Lucchini G, Piatti S. Mol Biol Cell. 20(10):2626-37. Pubmed
2008
- The spindle position checkpoint: how to deal with spindle misalignment during asymmetric cell division in budding yeast. Fraschini R, Venturetti M, Chiroli E, Piatti S. Biochem Soc Trans. 36(Pt 3):416-20. Pubmed
Régulation mitotique de la séparation des chromosomes et division cellulaire
Simonetta PIATTI
Cheffe d’équipe (Directrice de Recherche DR1 CNRS)
Membres de l’équipe
(IE-Recherche) (+33) 04 34 35 95 45 |
|
(CRCN) +33 (0)4 34 35 95 46 |
|
(Chercheur DR1) +33 (0)4 34 35 95 46 |
|
(IE-Recherche) +33 (0)4 34 35 95 48 |
|
(Doctorant) +33 (0)4 34 35 95 45 |
|
(Doctorant) +33 (0)4 34 35 95 45 |

Contactez notre équipe
Remplacez le nom et l’adresse ci-dessus par celui du membre à contacter
prenom.nom@crbm.cnrs.fr